aergf eartwertwnbedrtrtyudrtyhdtgsdjhhjzdsjjdsj

zsdtghfsgh stthg
srtesrtyeryt n edrt
journals such as Ann Surg, Ann Surg Oncol, Br J Surg and Hepatology. Also, part of this work has been presented in multiple international meetings, including ASA, SSO and AHPBA. Finally, Dimitrios is involved in state-of-the-art clinical research focusing on the role of liver transplantation in patients with primary and metastatic liver malignancies. Dimitrios has published high evidence data on the role of liver transplantation in patients with metastatic liver only disease of neuroendocrine or colorectal origin. Also, he is currently working on a multi-institutional study evaluating the role of Direct antiviral therapy on outcomes of patients with hepatitis C induced HCC undergoing liver transplantation. Of interest, Dimitrios is also leading a multi-institutional study using artificial intelligence and machine learning techniques to establish models to predict outcomes of patients undergoing liver transplantation for HCC within and beyond Milan Criteria (US HCC Liver transplant Collaborative).

There is no question that Dimitrios is an exceptionally accomplished clinical and basic science investigator having studied a large and broad number of topics in surgical oncology. He is currently one of the most prolific scientists at national level in the field of Liver neoplasms, that is certified by the international platform ‘’Experscape’’. This is an extraordinary accomplishment for a surgeon at his level of training and age. In fact, this stands out Dimitrios from most academic surgeons at his stage of career, it creates the expectation of better things to come from him in the future. This is the primary reason why I believe that he is such an outstanding candidate for the Cancers 2020 Young Investigator Award.
I think that this award will be well perceived by Dimitrios as a sign to continue his hard work to promote surgical science. I give him my highest recommendation.
Sincerely, ES Felekouras MD, PhD
Νευροενδοκρινείς όγκοι του Παγκρέατος (pNETs, pNENs)[1] – Ειδικό μέρος
Εισαγωγή
Τα pNETs είναι οι όγκοι της ενδοκρινούς μοίρας του παγκρέατος[2] και αποτελούσαν το 1-2% όλων των παγκρεατικών όγκων 1 αλλά σήμερα πιστεύουμε ότι είναι το 10% αυτών 2, 3. Η ετήσια επίπτωση τους στις ΗΠΑ ήταν 3,2 περιπτώσεις/106 πληθυσμού/έτος το 2003 αλλά το 2012 έφθασε το 8/106 4-6, και φαίνεται ότι συνεχίζουν να αυξάνονται 7. Εμφανίζονται κυρίως στην 4η με 6η δεκαετία της ζωής μας, με ελαφρά προτίμηση στους άνδρες (55%) 8.
Η χειρουργική θεραπεία των όγκων αυτών πέρασε και περνά από συνεχή εξέλιξη μια και οι όγκοι αυτοί είναι σπάνιοι όπως είπαμε, αλλά αυξάνονται, και έτσι χρειάσθηκε χρόνος για να μπορέσουμε να διαπιστώσουμε την λογική στρατηγική που πρέπει να ακολουθούμε στην θεραπεία τους.
Τα pNETs έχουν τη χειρότερη συνολική επιβίωση όλων των GEP-NETS, όπως αποδεικνύεται από την ανάλυση δεδομένων του SEER σε 49.012 GEP-NETs. Σε αυτή τη μελέτη 4, οι ασθενείς με pNETs είχαν 5-ετή επιβίωση 36,5%, αλλά η επιβίωση εξαρτάται επίσης από το στάδιο, και τα μικρά pNETs σε πρώιμο στάδιο έχουν εξαιρετική πρόγνωση. Σε αντίθεση με άλλα GEP-NETs, τα pNETs διαγιγνώσκονται συχνότερα σε υψηλότερο στάδιο με την παρουσία απομακρυσμένων μεταστάσεων έως και 40% κατά την παρουσίαση της νόσου, ίσως αντανακλώντας μια πιο επιθετική υποκείμενη βιολογική συμπεριφορά από άλλα GEP-NETs 4. Η διάμεση επιβίωση των ασθενών με pNET grade 1 και 2 είναι 42 μήνες. Σε όλους τους ασθενείς με pNETs εντοπισμένα στο πάγκρεας, η διάμεση επιβίωση είναι 136 μήνες, η οποία μειώνεται σε 77 μήνες όταν υπάρχουν λεμφαδενικές μεταστάσεις. Ωστόσο, το 64% των ασθενών παρουσιάζουν απομακρυσμένες μεταστάσεις (ήπαρ κ.λπ.) και σε αυτή την ομάδα, η διάμεση επιβίωση είναι μόνο 24 μήνες 5, 9. Πρακτικά το 80% των ασθενών με GEP-NETs και ειδικά pNETs είναι σταδίου IV κατά την διάγνωση και έχουν 5-ετή επιβίωση 35-65% με θνητότητα 2 φορές μεγαλύτερη από τους ασθενείς που έχουν μόνο τοπική νόσο 10.
Η προσέγγιση του ασθενούς με έναν τέτοιο όγκο πρέπει να είναι εξατομικευμένη κατά κάποιο τρόπο, ισορροπώντας μεταξύ της θεραπείας του κλινικού συνδρόμου υπερπαραγωγής ορμονών (αν υπάρχει), με τα συμπτώματα εκ της μάζας του όγκου. Η θεραπεία πρέπει να κατευθυνθεί όχι μόνο από την παρουσία συμπτωμάτων (ορμονικών ή μη), αλλά και από μια εκτίμηση της σχετικά μακράς φυσικής ιστορίας των όγκων αυτών. Ένα μεγάλο ποσοστό των pNETs, παραμένουν ασυμπτωματικοί όγκοι, όπως αποδεικνύεται από την επίπτωση αυτών των όγκων σε σειρές αυτοψίας (1.500/100.000) έναντι της χαμηλής κλινικής επίπτωσής τους (1/100.000) 11.
Κλινικά, στην αξιολόγηση των ασθενών με τους όγκους αυτούς, είναι σημαντικό να γίνει κατανοητό ότι, εκτός της ύπαρξης λειτουργικότητας ή όχι, φαίνεται να υπάρχουν δύο διαφορετικοί τύποι ασθενών με τέτοιους όγκους.
- Η πρώτη ομάδα αποτελείται από εκείνους τους ασθενείς που έχουν τους όγκους των χωρίς σημαντικές ενδοκρινικές διαταραχές στο προσωπικό ή οικογενειακό ιστορικό (σποραδικοί όγκοι) (> 85-95% των pNETs) 2, 12.
- Η δεύτερη ομάδα περιλαμβάνει εκείνους με σαφή ένδειξη μιας κληρονομούμενης προδιάθεσης με αυτοχρωμοσωματικό επικρατούντα χαρακτήρα στα πλαίσια ενδοκρινικού συνδρόμου όπως το Multiple Endocrine Neoplasia Type 1 (ΜΕΝ1) κυρίως, το σύνδρομο Von Hippel Lindau (VHL) και άλλα σύνδρομα 1, 13, 14_ENREF_2, όπως θα δούμε πιο κάτω (5-15% των pNETs) 2, 12.
Η διάγνωση όλων αυτών των όγκων εκτός από την κλινική εικόνα που δεν είναι ιδιαίτερα διαγνωστική για τον καθένα από αυτά, βασίζεται στις απεικονιστικές εξετάσεις, όσον αφορά τα μη λειτουργικά pNETs (NF-pNETs) και στην ανάπτυξη ακριβών μετρήσεων των ορμονών του πεπτικού στον ορό των ασθενών με ραδιοανοσολογικές μεθόδους (RIA, σε pg/mL) κ.α., όσον αφορά τα λειτουργικά pNETs (F-pNETs). Ιδιαίτερη βοήθεια στην διάγνωση και θεραπεία των συνδρόμων προσθέτουν οι διάφορες τεχνικές εντοπισμού των pNETs όταν δεν ανευρίσκονται με τις κλασσικές απεικονιστικές μεθόδους (Πίνακας 7, Γενικό Μέρος).
Τα GEP-NETs εκφράζουν υποδοχείς σωματοστατίνης σε > 80% των περιπτώσεων, που ανιχνεύονται με διάφορες μελέτες όπως π.χ. ανοσοϊστοχημεία ή λειτουργικές απεικονιστικές εξετάσεις FITs[3] όπως το Somatostatin Receptor Scintigraphy (SRS ή SRI)[4], (εμπορική ονομασία OctreoScan®) ή το 68Ga-DOTA-peptide Positron Emission Tomography (PET)/Computed Tomography (CT) (68Ga-DOTA-PET/CT) ή εν συντομία Ga PET/CT ή SSTR PET/CT 15, 16. Αυτή η ιδιαιτερότητα τους μας βοηθά ακόμα να ανιχνεύσουμε ασθενείς που μπορεί να ωφεληθούν από τα ανάλογα σωματοστατίνης (SSAs) ή από την θεραπεία με ραδιενεργά πεπτίδια (peptide receptors radionuclide therapy, PRRT) αν και τα SSAs δίδονται αρκετές φορές και με αρνητικές FITs 10.
Τα περισσότερα παγκρεατικά NETs (pNETs) είναι μονήρη, καλά αφοριζόμενα από τα πέριξ και είναι καλά διαφοροποιημένα νεοπλάσματα 17-19. Το μέγεθος τους είναι συνήθως μεταξύ 1-5 cm. Οι πολλαπλοί όγκοι είναι σπάνιοι και πρέπει πάντα όταν ανιχνεύονται, να γεννούν την υποψία κυρίως ΜΕΝ1 ή VHL 20. Το μέγεθος (> 2 cm), η διηθητική τοπική επέκταση, οι μεταστάσεις (λεμφαδένες και απομεμακρυσμένες), η αγγειακή διήθηση και η πολλαπλασιαστική τους δραστηριότητα στην βιοψία (Ki 67 κ.λπ.), καθορίζουν την πρόγνωση και την μεταστατική τους δυνατότητα. Αυτή η πολυπαραγοντική θεώρηση των διαφόρων μεταβλητών των όγκων αυτών είναι μια αξιόπιστη μέθοδος στην κατάταξη των όγκων αυτών σε ομάδες κίνδυνου 21. Ένας τέτοιος απλός παράγοντας κινδύνου από τους πολλούς, είναι το μέγεθος και σήμερα πιστεύουμε όλοι μας ότι τα 2 cm (διάμετρος) έχουν αρχίσει πλέον και αμφισβητούνται προς μικρότερα μεγέθη π.χ. 1,7 cm 22 και ίσως πρέπει να αναθεωρήσουμε το όριο των 2 cm για ένδειξη χειρουργικής επέμβασης αν και υπάρχουν αντίθετες απόψεις23.
Τα NF-pNETs παρατηρούνται συχνότερα από παλιότερα όπως είπαμε, αν και αυτό πιθανώς δεν απεικονίζει μια αληθινή αύξηση σε αριθμό, αλλά μάλλον βελτιωμένες διαγνωστικές μεθόδους 24. Από την άποψη της σχετικής συχνότητας αντιπροσωπεύουν τουλάχιστον το 60-80% όλων των pNETs .
Λειτουργικά και μη λειτουργικά pNETs εμφανίζονται σε ενηλίκους, αλλά με ευρύ όριο ηλικιών (20-80 έτη). Είναι σπάνια στα παιδιά 21. Τα περισσότερα είναι σποραδικά, αλλά μερικά μπορούν να εμφανιστούν στις κληρονομικές διαταραχές όπως στο ΜΕΝ1 την VHL και στην NF1 21. Τα παγκρεατικά νεοπλάσματα που χαρακτηρίζονται ως κακά διαφοροποιημένα pNECs, είναι σπάνια 18, 25. Τα φτωχά διαφοροποιημένα pNECs ταξινομούνται περαιτέρω ως μικροκυτταρικά καρκινώματα (small cell carcinomas) και μεγαλοκυτταρικά καρκινώματα (large cell carcinomas) με κύρια χαρακτηριστικά, την εκτεταμένη νέκρωση και πολλές μιτώσεις, και άφθονα αποπτωτικά σωμάτια. Τα πιο συχνά pNECs είναι τα μεγαλοκυτταρικά 26. Αυτά τα κακώς διαφοροποιημένα νευροενδοκρινικά καρκινώματα του παγκρέατος (pNECs) είναι επιθετικοί όγκοι και είναι συχνά ευρέως μεταστατικοί στη διάγνωση, και η θεραπεία σπάνια περιλαμβάνει χειρουργική εκτομή. Ως εκ τούτου, το κεφάλαιο αυτό δεν περιλαμβάνει pNECs, όπως και για τα MiNENs, αλλά επικεντρώνεται σε καλά διαφοροποιημένα pNETs.
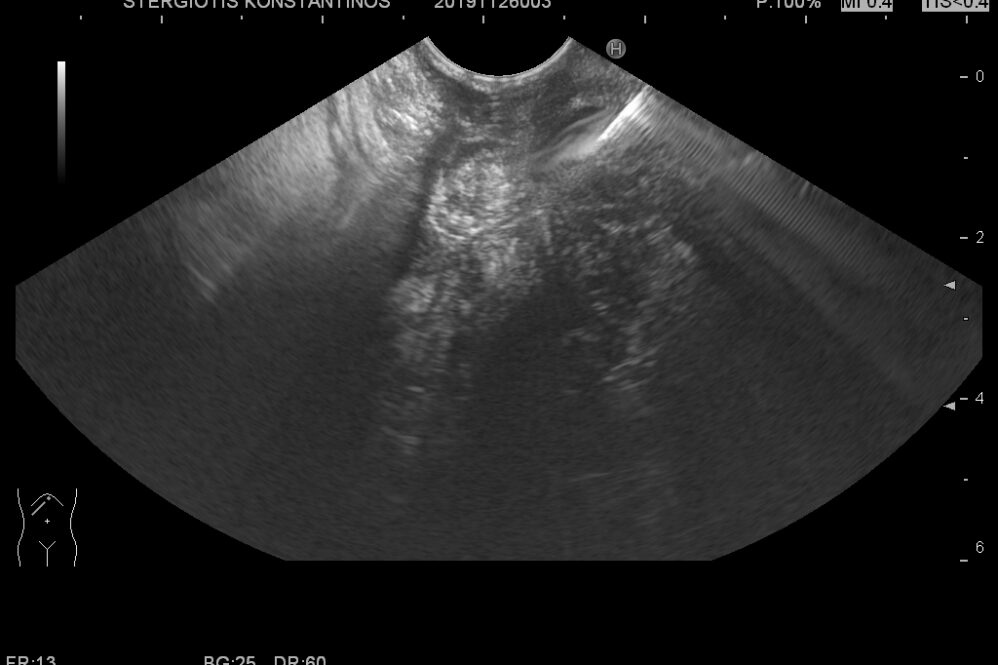
Τα παγκρεατικά NETs (pNETs) είναι περίπου το 3-10% όλων των παγκρεατικών νεοπλασμάτων 27, 28 και χαρακτηριστικά στις απεικονιστικές εξετάσεις δείχνουν ως να απωθούν τα πέριξ και έχουν χρώμα κίτρινο ή όπως η σάρκα του ψαριού ή μαύρο-καφέ χρώμα. Ορισμένοι όγκοι παρουσιάζουν πελίωση ή αιμορραγία και το 10% περίπου είναι μονόχωροι κυστικοί όγκοι με ινώδες υπόστρωμα στα πέριξ και περιέχουν κιτρινωπό κυστικό υγρό 29 30 31 (Εικόνα 1).
Εικόνα 1: Κυστικό pNET. Από 32.
Τα pNETs ανάλογα αν δημιουργούν ή όχι λειτουργικά συμπτώματα διακρίνονται στα λειτουργικά ή ορμονοπαραγωγά pNETs (F-pNETs) και στα μη λειτουργικά (NF-pNETs). Οι λειτουργικοί όγκοι παράγουν ποικιλία κλινικών συνδρόμων λόγω της υπερβολικής έκκρισης κάποιας ορμόνης, και αν και οι μη λειτουργικοί όγκοι μπορεί να παράγουν ορμόνες, αυτές δεν προκαλούν ένα κλινικά εμφανές σύνδρομο, τουλάχιστον στην αρχή της νόσου, αν και αυτό μπορεί να αλλάξει στην πορεία της νόσου. Οι τελευταίοι όγκοι είναι αυτοί που αποκαλούμε εκκριτικοί αλλά όχι λειτουργικοί (secretory but not functioning) 33.
Έτσι ένας κλινικός οδηγός για την καλύτερη διαχείριση των καλά διαφοροποιημένων pNETs (G1-G2-G3) μπορεί να έχει βάση τα κλινικά συμπτώματα που προκαλούνται από την τύχουν ορμονική υπερέκκριση ή όχι. Έτσι ο διαχωρισμός τους σε Λειτουργικά και μη Λειτουργικά pNETs που θεωρητικά μπορεί να μην είναι απόλυτα σωστός, μας βοηθά στην καλύτερη κατανόηση και διδασκαλία των όγκων αυτών (Πίνακας 1). Υπάρχουν 10 διαφορετικά κοινά αναγνωρισμένα pNETs, εκ των οποίων 9 σχετίζονται με ένα κλινικό σύνδρομο και μέχρι σήμερα έχουν βρεθεί και άλλα, σύνολο 14-15 (Πίνακας 2) αλλά είναι πιο σπάνια.
Πίνακας 1: Υπότυποι και τα πιο συχνά σύνδρομα των pNETs. Από 34.
Πίνακας 2: Η ταξινόμηση της WHO για τα GEP-NETs διαχρονικά μέχρι το 2017 35 (άνω) και το 2019 36 (κάτω).
Λειτουργικά (ορμονοπαραγωγά) pNETs και κλινικά σύνδρομα. (Functional Pancreatic Endocrine Tumors and Syndromes) (F-pNETs)
Γενικά
Τα σύνδρομα των λειτουργικών pNETs είναι αρκετά και φαίνονται στον Πίνακα 1, Γενικό Μέρος. H EΝΕΤs σε μια από τις πρόσφατες κατευθυντήριες οδηγίες της 37 δημοσίευσε ένα πίνακα με μια πιο λειτουργική κατάταξη με 14 σύνδρομα, αλλά πολλά είναι, αρκετά μέχρι πολύ σπάνια (Πίνακας 3).
- Ινσουλίνωμα
- Γαστρίνωμα
- Γλουκαγόνωμα ή γλυκαγόνωμα
- VIPωμα (VIP και VIPoma)
- Σπάνια pNETs
- Το Σωματοστατίνωμα 38
- Το Χολοκυστοκινίνωμα (CCK and CCKoma) 39
- Πολύ σπάνια λειτουργικά pNETs: Περιλαμβάνουν τα θετικά σε σεροτονίνη pNETs που προκαλούν καρκινοειδές σύνδρομο 34, 40 και ακόμα πιο σπάνια, τα θετικά σε ACTH pNETs που προκαλούν σύνδρομο Cushing 21, 41, τα growth hormone-releasing hormone (ή factor) GHRH pNETs που προκαλούν μεγαλακρία 21, 42, και άλλα θετικά σε parathyroid hormone-related peptide (PTHrP) που προκαλούν υπερασβεστιαιμία 43-49_ENREF_36 και ακόμα πιο σπάνια σε θετικά σε καλτσιτονίνη pNETs που προκαλούν διάρροια 50-52. Πολλά από αυτά τα νεοπλάσματα είναι μονήρη και μεγάλα και έχουν μεταστάσεις στο ήπαρ και τους λεμφαδένες όταν ανιχνεύονται. Η πρόγνωση είναι επομένως συνήθως φτωχή 17.
[1] Ο όρος NEN περιλαμβάνει καλά διαφοροποιημένους νευροενδοκρινικούς όγκους (NETs) και κακώς διαφοροποιημένα νευροενδοκρινικά καρκινώματα (NECs). Οι όροι NENs και NETs θα χρησιμοποιούνται σχεδόν αδιακρίτως στο κείμενο αυτό μια και η μέχρι τώρα βιβλιογραφία τα εμπεριείχε και τα δυο και μόνον τα τελευταία χρόνια αρχίσαν να ξεχωρίζουν.
[2] Είναι όγκοι προερχόμενοι εκ των ΝΕ κύτταρα των αδένων των εκφορητικών πόρων των παγκρεατικών πόρων και όχι απ’ ευθείας όγκοι των νησιδίων του παγκρέατος (islets). Για περισσότερες λεπτομέρειες μπορείτε να δείτε εδώ.
[3] FITs =Functional Imaging Techniques
[4] SRS=SRI. Οι όροι αυτοί θα χρησιμοποιούνται αδιακρίτως στο κείμενο αυτό.